En la actualidad, el denominado eje cerebro-intestino es uno de los campos más fértiles de la biomedicina. Se trata de una comunicación bidireccional entre el cerebro y las bacterias que tenemos en nuestro intestino a través de sustancias como vitaminas y hormonas que se mueven siguiendo la circulación de la sangre. Estos mensajes constantes no son una cuestión baladí, puesto que el intestino es el segundo órgano que contiene más neuronas y, además, es un importantísimo centro de regulación del sistema inmunitario, que nos protege de patógenos.
“Sabíamos que la microbiota puede influir en el cerebro, pero siempre a través de rutas indirectas, como el sistema inmune o la circulación sanguínea”. Celia Herrera-Rincón, investigadora Ramón y Cajal en la Facultad de Ciencias Biológicas de la Universidad Complutense de Madrid (UCM). Pero en su laboratorio han demostrado que una bacteria viva puede modificar directamente la actividad de una neurona con solo tocarla.
Es decir, que las neuronas no sólo notan la presencia de las bacterias, sino que también actúan en consecuencia y reaccionan emitiendo señales al propio interior de la célula o a sus compañeras a través de señales eléctricas. «Es un cambio de paradigma en nuestra forma de entender la comunicación entre microorganismos y el sistema nervioso», añade.
Formando un “minicerebro” en el laboratorio
Para lograr llevar a cabo su experimento, tomaron neuronas de un cerebro de rata y las sembraron en una placa de cultivo. Para «engañar» a las células y que creyesen que seguían en el interior de un organismo, añadieron medios de cultivo celular muy específicos y las situaron en un incubador a la temperatura del cuerpo. De este modo, las neuronas comenzaron a crecer y a dividirse durante 14 días hasta cubrir toda la superficie de crecimiento, interconectándose unas con otras.
Una vez tenían listo el minicerebro, añadieron al cultivo una bacteria característica de la microbiota humana: Lactiplantibacillus plantarum, que se encuentra en muchos alimentos y se considera beneficiosa para la salud. Así, dejaron que las bacterias crecieran junto a las neuronas y tomaron muestras en varios tiempos y para observar lo que iba sucediendo.
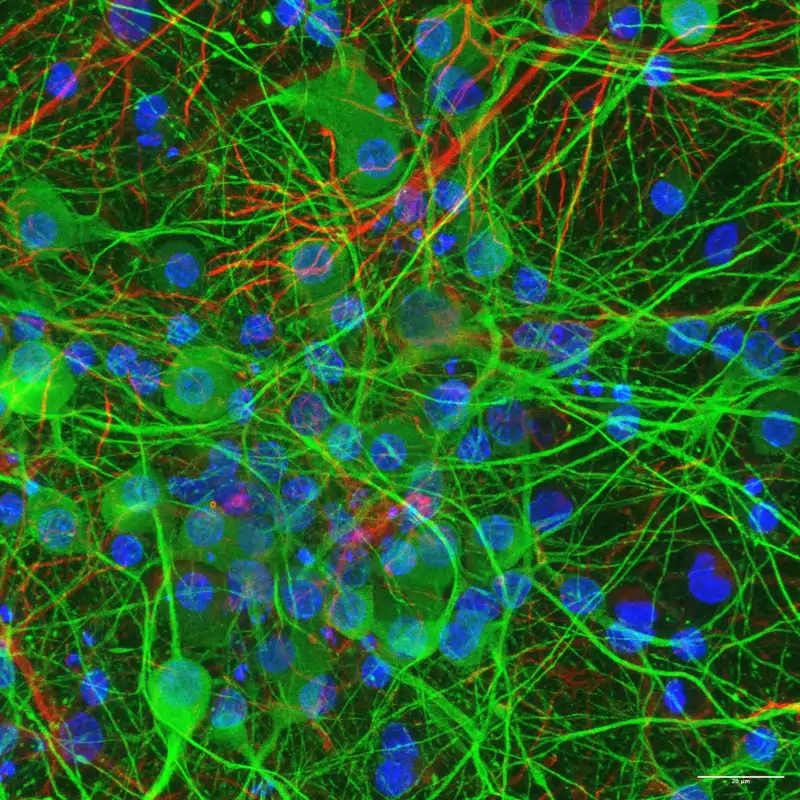
Mediante técnicas de microscopía avanzada y genéticas pudieron detectar cómo las bacterias se adhieren a la superficie de las neuronas, pero no las invaden. Es decir, se quedan «a las puertas» pero sin llegar a entrar en su interior. Aún sin entrar en las neuronas, su mera presencia induce ciertos cambios tanto en la actividad eléctrica como en la expresión de los genes de las neuronas. Unos cambios que podrían estar relacionados con la plasticidad neuronal, la inflamación o incluso algunas enfermedades. Es decir, que de alguna forma, estas bacterias están enviando mensajes a las neuronas, comunicándose con ellas.
Como comenta Juan Lombardo Hernández, investigador predoctoral y primer autor del artículo: «Es fascinante pensar que neuronas y bacterias, a pesar de pertenecer a reinos biológicos distintos, podrían compartir un lenguaje bioeléctrico común basado en canales iónicos y potenciales de membrana».
Cómo nos afecta este descubrimiento
Hay aproximadamente 100 billones de bacterias viviendo en nuestro intestino, cada una con sus cualidades. Por ello, estudiar la microbiota es una empresa extraordinariamente compleja, debido a la enorme cantidad de variables e interacciones que hay que tener en cuenta. En la actualidad apenas estamos comenzando a arañar la superficie de las implicaciones que supone tener a estas bacterias en nuestro interior y hasta qué punto condicionan nuestra salud o nuestra forma de pensar.
Aún con estas dificultades, las personas dedicadas al mundo de la investigación son muy capaces de resolver puzles aparentemente irresolubles y por ello, están poco a poco comprendiendo la función de la microbiota y lo que ocurre cuando se perturba. Estas perturbaciones pueden ocurrir por el uso de antibióticos, la dieta, o infecciones, y estudiar los cambios que ocurren puede ayudar a diseñar estrategias en el futuro que ayuden a patologías no sólo intestinales, sino también trastornos mentales o del sistema inmunitario.
Haber descubierto este nuevo modo de comunicación abre un camino más para comprender el papel de las bacterias intestinales en el sistema nervioso central. Se trata una visión holística del cuerpo, en el que las partes funcionan como un todo interconectado. Con esta premisa, el estudio podría acabar derivando en futuras terapias neuroactivas basadas en bacterias vivas o inactivadas que mejoren nuestra salud.
via Daniel Pellicer Roig https://ift.tt/XxaRTuV
No hay comentarios:
Publicar un comentario